kapalı
Sitenizi Seçin
Küresel
Sosyal Medya


Görüntüleme: 0 Yazar: Site Editörü Yayınlanma Tarihi: 2025-07-02 Kaynak: Alan
Kimyasal reaksiyon kalsiyumdan kalsiyum okside basittir. Kalsiyum metali oksijen gazıyla reaksiyona girer. Dengeli denklem:
2Ca + O₂ → 2CaO
Bu reaksiyon kalsiyum oksit oluşturur. Kalsiyum oksit birçok endüstri için önemlidir. Kalsiyumdan kalsiyum oksit elde etmenin iki ana yolu vardır. Bunun bir yolu kalsiyumun oksijenle reaksiyona sokulmasıdır. Diğer yol ise kalsiyum karbonatın ısıtılmasıdır. İnşaat ve çelik endüstrileri çok fazla kalsiyum oksit kullanıyor. Ayrıca çevreye yardımcı olmak için de kullanılır. Changshu Hongyu gibi şirketler kalsiyum hidroksit ve kalsiyum karbonat gibi ürünler üretiyor. Bu ürünlere dünya çapında daha fazla ihtiyaç duyulmaktadır.
Kalsiyum oksit üretme süreci basittir ve öncelikle kalsiyum karbonatın (kireç taşı) ısıtılarak kalsiyum oksit (sönmemiş kireç) oluşturulmasını içerir. Bu reaksiyon kalsinasyon olarak bilinir. Her ne kadar kalsiyum metali oksijenle reaksiyona girerek kalsiyum oksit oluşturabilse de bu yaygın endüstriyel yöntem değildir. Bunun yerine, büyük ölçekte kalsiyum oksit üretmenin ana yaklaşımı, kalsiyum karbonatın ısıtılmasıdır. Bu yöntem inşaat, çelik ve çevre koruma gibi birçok endüstri için çok önemlidir.
Kalsinasyon Süreci ve Kimyasal Denklem
Kalsiyum oksit üretmek için birincil kimyasal reaksiyon aşağıdaki gibidir:
CaCO3(ler)→CaO(lar)+CO2(g)
Bu işlemde, kalsiyum karbonat (CaCO₃) bir fırın veya fırında ısıtılır ve burada kalsiyum oksit (CaO) ve karbondioksit (CO₂) gazına ayrışır. Kalsinasyon sırasında sağlanan yüksek ısı, kalsiyum karbonatı bu iki ürüne ayırır.
Kalsiyum oksijenle hızlı reaksiyona girer ve kalsiyum oksit . Kalsiyum oksit beyaz bir tozdur. Birçok endüstri bu tozu kullanıyor. Kalsiyum oksit elde etmenin ana yolu kalsiyum karbonatın ısıtılmasıdır. Bu işleme kalsinasyon denir. Kalsiyum oksit çimento yapımında çok önemlidir. Gazların temizlenmesine ve suyun arıtılmasına yardımcı olur. Ayrıca toprağın daha iyi olmasına yardımcı olur. Kalsiyum oksitle çalışırken güvenlik ekipmanı giymeniz gerekir. Eldivenler ve gözlükler cildinizi, gözlerinizi ve ciğerlerinizi korur. Changshu Hongyu gibi şirketler iyi kalsiyum oksit üretiyor. Sıkı güvenlik ve çevre kuralları uyguluyorlar.

Kalsiyumun kalsiyum okside dönüştürülmesi basit bir işlemdir. Bu, kalsiyum metali havadaki oksijene temas ettiğinde meydana gelir. Doğru atom sayısını gösterecek şekilde denklemin dengelenmesi gerekir. Denklemi şu şekilde dengeleyebilirsiniz:
Dengesiz denklemle başlayın: Ca + O₂ → CaO.
Her iki taraftaki atomları sayın. Sol tarafta 1 kalsiyum ve 2 oksijen atomu vardır. Sağ tarafta 1 kalsiyum ve 1 oksijen atomu bulunur.
Oksijeni sabitlemek için CaO'nun önüne 2 koyun: Ca + O₂ → 2CaO.
Daha sonra Ca'nın önüne 2 ekleyin: 2Ca + O₂ → 2CaO.
Nihai dengeli denklem şu şekildedir:
2Ca + O₂ → 2CaO
Bu, iki kalsiyum atomunun bir oksijen molekülüyle reaksiyona girerek iki kalsiyum oksit birimi oluşturduğu anlamına gelir. Bu bir sentez reaksiyonudur. Yeni bir bileşik oluşturmak için iki element birleşir.
Kalsiyum havada yandığında oksijenle reaksiyona girer. Bu beyaz bir toz olan kalsiyum oksit yapar. Birçok endüstri bu tozu kullanıyor. Reaksiyon çok fazla ısı ve ışık yayar. Enerji açığa çıkardığı için ekzotermik olarak adlandırılır. Bilim adamları bu reaksiyonun ne kadar enerji açığa çıkardığını araştırdılar. Kalsiyum oksidin standart oluşum entalpisi yaklaşık -624,5 kJ/mol'dür. Bu, reaksiyonun çok fazla enerji açığa çıkardığı anlamına gelir. Reaksiyonun hızlı ve tam olmasının nedeni budur.
Not: Bu reaksiyonu yalnızca profesyoneller yapmalıdır. Çok fazla ısı ve parlak ışık ürettiği için tehlikeli olabilir.
Kalsiyumdan kalsiyum okside kimyasal reaksiyon bilim ve endüstri için önemlidir. Changshu Hongyu gibi şirketler bu reaksiyonu yüksek saflıkta kalsiyum oksit yapmak için kullanıyor. Kalsiyum hidroksit ve kalsiyum karbonat gibi ürünleri birçok endüstriye yardımcı olmaktadır. Bunlara inşaat, çevre koruma ve tıp dahildir.
Bu reaksiyonun diğer yöntemlerle nasıl karşılaştırıldığını görmek için şu tabloya bakın:
Bakış açısı |
Doğrudan Reaksiyon (Kalsiyum + Oksijen) |
Kalsiyum Karbonatın Kalsinasyonu |
|---|---|---|
Reaksiyon Mekanizması |
Kalsiyum doğrudan oksijenle reaksiyona girerek CaO oluşturur |
Kalsiyum karbonat CaO ve CO₂'ye ayrışır |
Sıcaklık Aralığı |
Yüksek sıcaklıklarda meydana gelir |
850–1000 °C gerektirir |
Yeterlik |
Yüksek verimli, hızlı reaksiyon |
Verimli ancak CO₂ basıncına bağlıdır |
Ürün Reaktivitesi |
Yüksek saflıkta kalsiyum oksit oluşturur |
Reaktiviteyi artıran gözenekli CaO üretir |
Endüstriyel Kullanım |
Büyük ölçekli üretim için daha az yaygın |
Endüstriyel kalsiyum oksit için ana yöntem |
Kalsiyumun kalsiyum okside reaksiyonu hızlıdır ve çok fazla enerji açığa çıkar. Ancak çoğu endüstri, büyük miktarlarda kalsiyum oksit yapmak için kalsiyum karbonatın kalsinasyonunu kullanır. Her iki yol da kalsiyum oksit üretir. Seçim, ürünün kalitesine ve sürecin ne kadar verimli olduğuna bağlıdır.
Kalsiyum oksit, inşaat malzemelerinin yapımında ve suyun arıtılmasında önemlidir. Aynı zamanda kimyasal üretime de yardımcı olur. Kalsiyum oksit oluşturan reaksiyon diğer birçok işlemde kullanılır. Bunlara kalsiyum hidroksit ve hafif kalsiyum karbonat yapımı da dahildir. Changshu Hongyu her kalsiyum oksit partisini kalite açısından kontrol ediyor. Bu, ürünlerine dünya çapındaki müşteriler tarafından güvenilmesini sağlar.

Kalsinasyon fabrikalarda önemli bir süreçtir. Kalsiyum karbonatı kalsiyum okside dönüştürür. İşçiler kireçtaşını veya diğer malzemeleri kalsiyum karbonatla bir fırında ısıtırlar. Isı kimyasal bir reaksiyonu başlatır. Bu reaksiyonda kalsiyum karbonat, kalsiyum oksit ve karbondioksit gazına ayrışır. Reaksiyon şu şekilde görünür:
CaCO₃(ler) → CaO(lar) + CO₂(g)
Bu reaksiyon, kalsiyum oksidin diğer adı olan sönmemiş kireci oluşturur. Bu işlem sırasında malzeme erimez. Yüksek ısı onu parçalara ayırır. Karbondioksit gazı fırından çıkar. Katı kalsiyum oksit geride kalır. İşçiler kalsiyum oksitle hızlı bir şekilde ilgilenmezse havadaki karbondioksitle reaksiyona girebilir. Daha sonra tekrar kalsiyum karbonata dönüşür. Birçok fabrika bu reaksiyonu bol miktarda kalsiyum oksit üretmek için kullanır. Çimento ve çelik gibi şeyler için kullanıyorlar.
Not: Kalsinasyon işlemi büyük miktarlarda kalsiyum oksit üretmenin ana yoludur. Kalsiyumun oksijenle doğrudan reaksiyonundan daha iyi çalışır.
Kalsinasyon işlemi ısı ve havanın dikkatli kontrolünü gerektirir. Reaksiyon yaklaşık 640°C'de başlar. Havada yapıldığında 825°C civarında tamamlanır. Çoğu fabrika, ısıyı sabit tutmak için döner fırınlar veya kalsinatörler kullanır. Bu makineler malzemeyi yaklaşık 850°C'ye ısıtır. Bu, reaksiyonun tamamlandığından emin olmanızı sağlar.
İşlem en iyi şekilde bol oksijenle veya kontrollü bir alanda çalışır.
Fırın malzemenin erimesini önlemelidir.
Reaksiyon, çevreye yardımcı olmak için yönetilmesi gereken karbondioksit üretir.
Modern fırınlar her ton kalsiyum oksit için yaklaşık 3,75 gigajul enerji kullanır. Ayrıca ton başına yaklaşık 20 kilovatsaat elektrik kullanıyorlar. Changshu Hongyu gibi şirketler süreci kontrol etmek için yeni teknoloji kullanıyor. Bu daha iyi ürünler üretilmesine yardımcı olur. Ayrıca emisyonları azaltmaya ve yan ürünleri akıllı yöntemlerle kullanmaya çalışıyorlar. Ana yan ürün olan karbondioksit genellikle çevreyi korumak için yakalanıyor veya başka işlerde kullanılıyor.
Yeni fikirler arasında kalsiyum oksit nanopartikülleri yapmak için yeşil yolların kullanılması yer alıyor. Otomasyon aynı zamanda sürecin daha iyi hale getirilmesine de yardımcı olur. Bu adımlar şirketlerin katı çevre kurallarına uymasına yardımcı olur. Ayrıca inşaat, çiftçilik ve tıp için yüksek saflıkta ürünler üretiyorlar. Changshu Hongyu'nun kalsinasyon ve kalsiyum hidroksit gibi ilgili ürünlerdeki becerisi ve kalsiyum karbonat , dünya çapında birçok endüstriye yardımcı olur.
Kalsiyum oksit birçok endüstride çok önemlidir. İnşaatta işçiler bunu çimento yapmak için kullanıyor. Klinker yapmak için kil ve suyla karışır. Daha sonra klinker öğütülerek çimento tozu haline getirilir. İnşaatçılar ayrıca harç ve sıvada da kullanırlar. Onu, güçlü binaların yapılmasına yardımcı olan kalsiyum hidroksite dönüştürürler. Yüksek ısı direnci ve suyla reaksiyona girmesi beton yapımında faydalıdır.
Kalsiyum hidroksit oluşturmak üzere suyla reaksiyona girerek harç ve beton yapılmasına yardımcı olur.
Yollar, köprüler ve binalar için çimento yapmak gerekir.
Kimya endüstrisinde kalsiyum oksit, kükürt dioksitin gazlardan uzaklaştırılmasına yardımcı olur. Enerji santralleri ve fabrikalar bunu havayı temizlemek için kullanıyor. Temiz hava kurallarının karşılanmasına yardımcı olmak için asitli gazlarla reaksiyona girer.
PH'ı kontrol etmeye ve kötü gazları nötralize etmeye yardımcı olur.
Yan ürün olarak inşaatta kullanılan alçıyı üretir.
Çevre için, su ve toprağı arıtmak için kalsiyum oksit kullanılır. Kireç hayvan atıklarını, kanalizasyonu ve fabrika çamurunu arıtır. Ağır metallerin sabitlenmesine yardımcı olur, atık sudaki pH değerini değiştirir ve suyu yumuşatır. Madencilikte asit maden drenajına yardımcı olur ve toprağı daha iyi hale getirir.
Suyun temizlenmesine ve toprağın sabitlenmesine yardımcı olarak yerleri daha güvenli hale getirir.
Kalsiyum oksit aynı zamanda metal yapımında da kullanılır. Çelik ve alüminyumdaki kötü maddelerin uzaklaştırılmasına yardımcı olur. Bu metali daha iyi hale getirir. Aşağıdaki grafik farklı ülkelerin ne kadar çelik ürettiğini göstermektedir, bu da kalsiyum oksit ihtiyacını artırmaktadır.
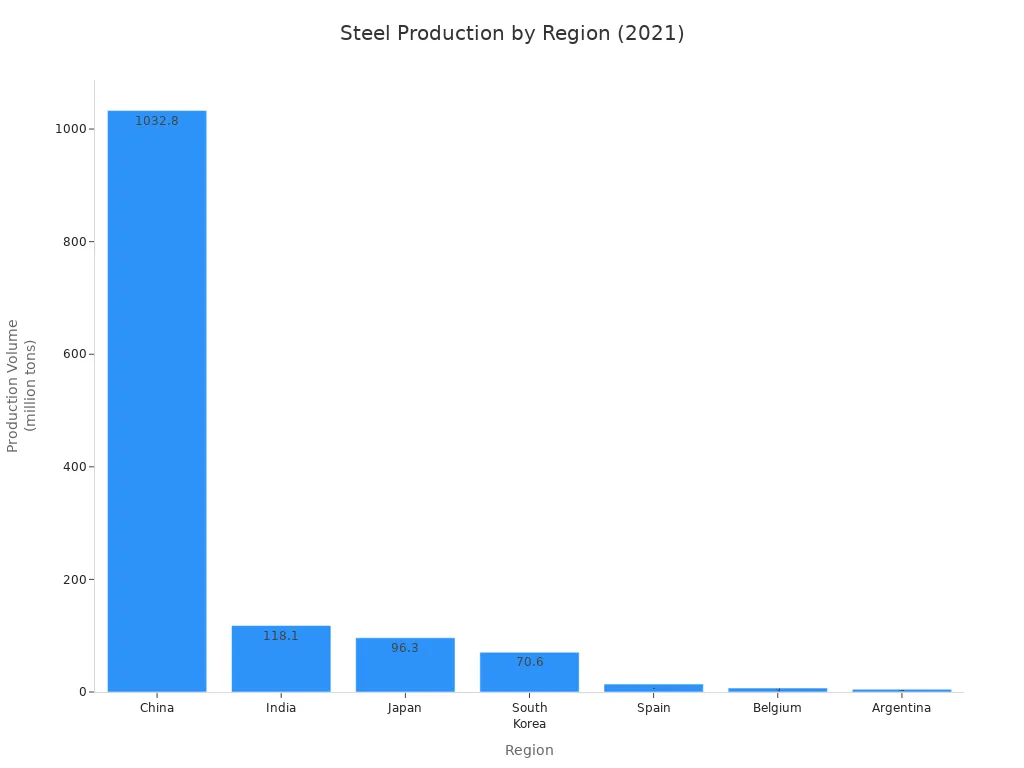
İnsanlar kalsiyum oksitle çalışırken dikkatli olmalıdır. Cildinize, gözlerinize ve ciğerlerinize zarar verebilir. İşçiler gözlerini korumak için koruyucu gözlük takmalıdır. Derilerinden uzak tutmak için eldiven ve özel kıyafetler kullanmaları gerekir.
Toz veya duman varsa solunum cihazı kullanın.
Toz yapmayın ve solumayın.
Çalışma alanlarının iyi hava akışına sahip olduğundan emin olun.
Kalsiyum oksidi serin ve kuru, iyi hava alan bir yerde saklayın. Kapları sıkıca kapalı ve sudan uzak tutun. Yemek yemeden veya işten ayrılmadan önce ellerinizi yıkayın. Saklama ve atma konusunda tüm yerel kurallara uyun.
İpucu: Kalsiyum oksit veya kalsiyum hidroksit ve kalsiyum karbonat gibi ilgili ürünlerle çalışırken daima güvenlik ekipmanı kullanın ve kurallara uyun.
Changshu Hongyu, ürünlerinin güvenli ve kaliteli olmasını sağlar. ABD Kalsiyum oksitleri , Avrupa ve Japonya'daki kurallara uygundur. Bu, gıdada, ilaçta ve çevreye yardımda kullanılabileceği anlamına gelir.
Kalsiyum oksijenle reaksiyona girdiğinde veya kalsiyum karbonat ısıtıldığında kalsiyum oksit oluşur.
Fabrikalar bu işlemi çelik, cam ve temizleme suyu için sönmemiş kireç yapmak amacıyla kullanır.
Kalsiyum oksit ayrıca çimentoda, toprakta ve evde kullanılan eşyalarda da bulunur.
Changshu Hongyu gibi şirketler, kalsiyum oksit, kalsiyum hidroksit ve kalsiyum karbonatın dünyanın her yerindeki insanlar için güvenli ve iyi olduğundan emin oluyorlar.
Yeni makineler ve fikirler artık bu ürünlerin daha güvenli ve temiz yöntemlerle üretilmesine yardımcı oluyor; bu da gelecek için daha iyi.
Çimento yapımında kalsiyum oksit kullanılır. Aynı zamanda fabrikalardaki suyu arıtır ve gazları temizler. Birçok çelik fabrikası da bunu kullanıyor. Changshu Hongyu bu işler için saf kalsiyum oksit satıyor.
Kalsiyum oksit suyla karışarak kalsiyum hidroksit oluşturur. Kalsiyum hidroksit daha yumuşaktır ve suda daha iyi karışır. Her ikisi de çevreyi inşa etmek ve ona yardım etmek için önemlidir.
Kalsiyum oksit cildinizi, gözlerinizi ve ciğerlerinizi rahatsız edebilir. İnsanlar bunu kullanırken eldiven, gözlük ve maske takmalıdır. Changshu Hongyu, insanları güvende tutmak ve iyi ürünler üretmek için güçlü güvenlik kuralları kullanıyor.
Çoğu fabrika ana malzeme olarak kireçtaşı kullanır. Kireçtaşının içinde kalsiyum karbonat bulunur. Kireçtaşının ısıtılması kalsiyum oksit ve karbondioksit üretir. Buna kalsinasyon denir.
Müşteriler kalsiyum oksit ve diğer ürünleri satın almak için Changshu Hongyu'nun web sitesine gidebilirler. Şirket iyi hizmet veriyor ve dünyanın her yerindeki alıcılara yardımcı oluyor.