dichtbij
Kies uw site
Globaal
Sociale media


Aantal keren bekeken: 0 Auteur: Site-editor Publicatietijd: 02-07-2025 Herkomst: Locatie
De chemische reactie van calcium naar calciumoxide is eenvoudig. Calciummetaal reageert met zuurstofgas. De evenwichtige vergelijking is:
2Ca + O₂ → 2CaO
Bij deze reactie ontstaat calciumoxide. Calciumoxide is belangrijk voor veel industrieën. Er zijn twee manieren om calciumoxide uit calcium te maken. Eén manier is het laten reageren van calcium met zuurstof. De andere manier is het verwarmen van calciumcarbonaat. De bouw- en staalindustrie gebruikt veel calciumoxide. Het wordt ook gebruikt om het milieu te helpen. Bedrijven als Changshu Hongyu maken producten zoals calciumhydroxide en calciumcarbonaat. Deze producten zijn over de hele wereld steeds meer nodig.
Het productieproces van calciumoxide is eenvoudig en omvat voornamelijk de verhitting van calciumcarbonaat (kalksteen) om calciumoxide (ongebluste kalk) te vormen. Deze reactie staat bekend als calcineren. Hoewel calciummetaal ook met zuurstof kan reageren om calciumoxide te vormen, is dit niet de gebruikelijke industriële methode. In plaats daarvan is de belangrijkste aanpak voor het op grote schaal produceren van calciumoxide het verwarmen van calciumcarbonaat. Deze methode is van cruciaal belang voor veel industrieën, zoals de bouw-, staal- en milieubescherming.
Calcinatieproces en chemische vergelijking
De primaire chemische reactie voor het produceren van calciumoxide is als volgt:
CaCO3(s) →CaO(s)+CO2(g)
Bij dit proces wordt calciumcarbonaat (CaCO₃) verwarmd in een oven, waar het uiteenvalt in calciumoxide (CaO) en kooldioxide (CO₂). De hoge hitte die tijdens het calcineren vrijkomt, breekt calciumcarbonaat af in deze twee producten.
Calcium reageert snel met zuurstof en maakt calciumoxide . Calciumoxide is een wit poeder. Veel industrieën gebruiken dit poeder. De belangrijkste manier om calciumoxide te verkrijgen is door calciumcarbonaat te verwarmen. Dit proces wordt calcineren genoemd. Calciumoxide is erg belangrijk voor het maken van cement. Het helpt bij het reinigen van gassen en het behandelen van water. Het helpt ook om de bodem beter te maken. U moet veiligheidsuitrusting dragen als u met calciumoxide werkt. Handschoenen en een veiligheidsbril beschermen uw huid, ogen en longen. Bedrijven als Changshu Hongyu maken goed calciumoxide. Zij hanteren strikte veiligheids- en milieuregels.

Het veranderen van calcium in calciumoxide is een eenvoudig proces. Dit gebeurt wanneer calciummetaal zuurstof in de lucht raakt. De vergelijking moet in evenwicht zijn om het juiste aantal atomen weer te geven. Hier ziet u hoe u de vergelijking in evenwicht brengt:
Begin met de ongebalanceerde vergelijking: Ca + O₂ → CaO.
Tel de atomen aan elke kant. De linkerkant heeft 1 calcium- en 2 zuurstofatomen. De rechterkant heeft 1 calcium- en 1 zuurstofatoom.
Om de zuurstof te fixeren zet je een 2 voor CaO: Ca + O₂ → 2CaO.
Zet vervolgens een 2 voor Ca: 2Ca + O₂ → 2CaO.
De uiteindelijke uitgebalanceerde vergelijking is:
2Ca + O₂ → 2CaO
Dit betekent dat twee calciumatomen reageren met één zuurstofmolecuul om twee calciumoxide-eenheden te maken. Dit is een synthesereactie. Twee elementen komen samen om een nieuwe verbinding te vormen.
Calcium reageert met zuurstof wanneer het in de lucht verbrandt. Hierdoor ontstaat calciumoxide, een wit poeder. Veel industrieën gebruiken dit poeder. Bij de reactie komt veel warmte en licht vrij. Het wordt exotherm genoemd omdat er energie vrijkomt. Wetenschappers hebben onderzocht hoeveel energie deze reactie vrijgeeft. De standaard vormingsenthalpie voor calciumoxide bedraagt ongeveer -624,5 kJ/mol. Dit betekent dat bij de reactie veel energie vrijkomt. Daarom is de reactie snel en volledig.
Opmerking: alleen professionals mogen deze reactie uitvoeren. Het kan gevaarlijk zijn omdat het veel hitte en fel licht produceert.
De chemische reactie van calcium tot calciumoxide is belangrijk voor wetenschap en industrie. Bedrijven als Changshu Hongyu gebruiken deze reactie om zeer zuiver calciumoxide te maken. Hun producten, zoals calciumhydroxide en calciumcarbonaat, helpen veel industrieën. Deze omvatten de bouw, milieubescherming en geneeskunde.
Bekijk deze tabel om te zien hoe deze reactie zich verhoudt tot andere manieren:
Aspect |
Directe reactie (calcium + zuurstof) |
Calcineren van calciumcarbonaat |
|---|---|---|
Reactiemechanisme |
Calcium reageert direct met zuurstof en vormt CaO |
Calciumcarbonaat ontleedt tot CaO en CO₂ |
Temperatuurbereik |
Komt voor bij hoge temperaturen |
Vereist 850–1000 °C |
Efficiëntie |
Zeer efficiënte, snelle reactie |
Efficiënt, maar afhankelijk van de CO₂-druk |
Productreactiviteit |
Vormt calciumoxide met een hoge zuiverheid |
Produceert poreus CaO, waardoor de reactiviteit wordt verbeterd |
Industrieel gebruik |
Minder gebruikelijk voor grootschalige productie |
Belangrijkste methode voor industrieel calciumoxide |
De reactie van calcium naar calciumoxide verloopt snel en geeft veel energie. Maar de meeste industrieën gebruiken het calcineren van calciumcarbonaat om calciumoxide in grote hoeveelheden te maken. Beide manieren maken calciumoxide. De keuze hangt af van de productkwaliteit en hoe efficiënt het proces is.
Calciumoxide is belangrijk voor het maken van bouwmaterialen en het behandelen van water. Het helpt ook bij de chemische productie. De reactie die calciumoxide maakt, wordt in veel andere processen gebruikt. Deze omvatten het maken van calciumhydroxide en licht calciumcarbonaat. Changshu Hongyu controleert elke partij calciumoxide op kwaliteit. Hierdoor worden hun producten vertrouwd door klanten over de hele wereld.

Calcineren is een belangrijk proces in fabrieken. Het verandert calciumcarbonaat in calciumoxide. andert calciumcarbonaat in calciumoxide. Werknemers verwarmen kalksteen of andere materialen met calciumcarbonaat in een oven. Door de hitte ontstaat er een chemische reactie. Bij deze reactie wordt calciumcarbonaat afgebroken tot calciumoxide en kooldioxidegas. De reactie ziet er als volgt uit:
CaCO₃(s) → CaO(s) + CO₂(g)
Bij deze reactie ontstaat ongebluste kalk, een andere naam voor calciumoxide. Het materiaal smelt tijdens dit proces niet. Hoge hitte breekt het uit elkaar. Het kooldioxidegas verlaat de oven. Het vaste calciumoxide blijft achter. Als werknemers niet snel met het calciumoxide omgaan, kan het reageren met kooldioxide in de lucht. Dan verandert het weer in calciumcarbonaat. Veel fabrieken gebruiken deze reactie om veel calciumoxide te maken. Ze gebruiken het voor zaken als cement en staal.
Opmerking: Het calcinatieproces is de belangrijkste manier om calciumoxide in grote hoeveelheden te maken. Het werkt beter dan de directe reactie van calcium met zuurstof.
Het calcinatieproces vereist een zorgvuldige controle van warmte en lucht. De reactie begint bij ongeveer 640°C. Wanneer het aan de lucht wordt gedaan, eindigt het bij een temperatuur van 825°C. De meeste fabrieken gebruiken roterende ovens of calciners om de hitte stabiel te houden. Deze machines verwarmen het materiaal tot ongeveer 850°C. Dit zorgt ervoor dat de reactie voltooid is.
Het proces werkt het beste met veel zuurstof of in een gecontroleerde ruimte.
De oven moet voorkomen dat het materiaal smelt.
Bij de reactie ontstaat koolstofdioxide, die moet worden beheerd om het milieu te helpen.
Moderne ovens gebruiken ongeveer 3,75 gigajoule energie voor elke ton calciumoxide. Ze gebruiken ook ongeveer 20 kilowattuur elektriciteit per ton. Bedrijven als Changshu Hongyu gebruiken nieuwe technologie om het proces te beheersen. Dit helpt om betere producten te maken. Ze proberen ook de uitstoot te verlagen en bijproducten op slimme manieren te gebruiken. Het belangrijkste bijproduct, koolstofdioxide, wordt vaak opgevangen of gebruikt in andere banen om het milieu te beschermen.
Nieuwe ideeën zijn onder meer het gebruik van groene manieren om calciumoxide-nanodeeltjes te maken. Automatisering helpt ook om het proces te verbeteren. Deze stappen helpen bedrijven om strikte milieuregels te volgen. Ze maken ook zeer zuivere producten voor de bouw, landbouw en geneeskunde. Changshu Hongyu's vaardigheid in calcineren en aanverwante producten, zoals calciumhydroxide en calciumcarbonaat helpt veel industrieën over de hele wereld.
Calciumoxide is in veel industrieën erg belangrijk. In de bouw gebruiken arbeiders het om cement te maken. Het vermengt zich met klei en water om klinker te maken. Vervolgens wordt de klinker vermalen tot cementpoeder. Bouwers gebruiken het ook in mortel en gips. Ze veranderen het in calciumhydroxide, wat helpt bij het maken van sterke gebouwen. De hoge hittebestendigheid en de reactie met water zijn nuttig bij het maken van beton.
Het helpt bij het maken van mortel en beton door te reageren met water om calciumhydroxide te vormen.
Het is nodig om cement te maken voor wegen, bruggen en gebouwen.
In de chemische industrie helpt calciumoxide zwaveldioxide uit gassen te verwijderen. Elektriciteitscentrales en fabrieken gebruiken het om de lucht te zuiveren. Het reageert met zure gassen om te helpen voldoen aan de regels voor schone lucht.
Het helpt de pH onder controle te houden en slechte gassen te neutraliseren.
Als bijproduct wordt gips gemaakt, dat in de bouw wordt gebruikt.
Voor het milieu wordt calciumoxide gebruikt om water en bodem te behandelen. Kalk behandelt dierlijk afval, rioolwater en fabrieksslib. Het helpt zware metalen te fixeren, verandert de pH in afvalwater en verzacht water. In de mijnbouw helpt het bij de zure mijndrainage en maakt het de bodem beter.
Het helpt water schoon te maken en de bodem te fixeren, waardoor plaatsen veiliger worden.
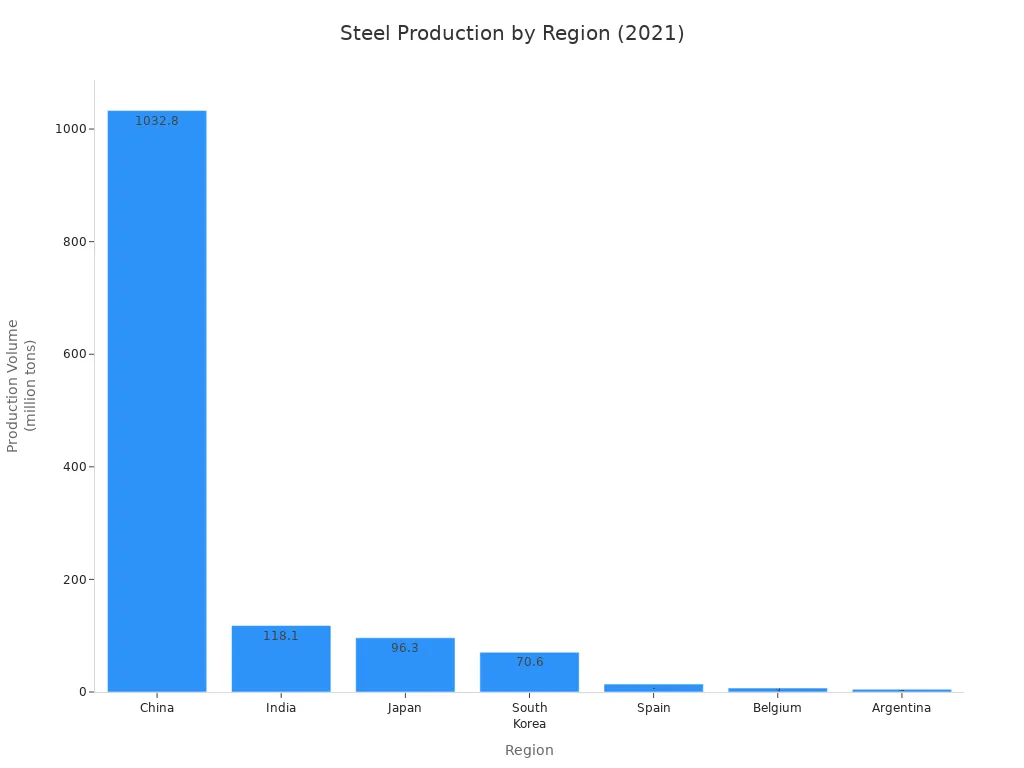
Calciumoxide wordt ook gebruikt bij het maken van metalen. Het helpt bij het verwijderen van slechte stoffen uit staal en aluminium. Hierdoor wordt het metaal beter. Onderstaande grafiek laat zien hoeveel staal verschillende landen produceren, waardoor de behoefte aan calciumoxide toeneemt.
Mensen moeten voorzichtig zijn bij het omgaan met calciumoxide. Het kan uw huid, ogen en longen beschadigen. Werknemers moeten een veiligheidsbril dragen om hun ogen te beschermen. Ze moeten handschoenen en speciale kleding gebruiken om het van hun huid te houden.
Gebruik een gasmasker als er stof of dampen aanwezig zijn.
Maak geen stof en adem het niet in.
Zorg ervoor dat de werkplekken een goede luchtstroom hebben.
Bewaar calciumoxide op een koele, droge plaats met goede lucht. Houd containers goed gesloten en uit de buurt van water. Was uw handen voordat u gaat eten of het werk verlaat. Volg alle lokale regels voor het opslaan en weggooien.
Tip: Gebruik altijd veiligheidsuitrusting en volg de regels bij het werken met calciumoxide of aanverwante producten zoals calciumhydroxide en calciumcarbonaat.
Changshu Hongyu zorgt ervoor dat hun producten veilig en van hoge kwaliteit zijn. Hun calciumoxide voldoet aan de regels in de VS, Europa en Japan. Dit betekent dat het kan worden gebruikt in voedsel, medicijnen en om het milieu te helpen.
Wanneer calcium reageert met zuurstof of wanneer calciumcarbonaat wordt verwarmd, ontstaat calciumoxide.
Fabrieken gebruiken dit proces om ongebluste kalk te maken voor staal, glas en schoonmaakwater.
Calciumoxide wordt ook aangetroffen in cement, grondfixatie en dingen die thuis worden gebruikt.
Bedrijven zoals Changshu Hongyu zorgen ervoor dat hun calciumoxide, calciumhydroxide en calciumcarbonaat veilig en goed zijn voor mensen overal ter wereld.
Nieuwe machines en ideeën helpen deze producten nu op veiligere en schonere manieren te maken, wat beter is voor de toekomst.
Calciumoxide wordt gebruikt om cement te maken. Het behandelt ook water en reinigt gassen uit fabrieken. Veel staalfabrieken maken er ook gebruik van. Changshu Hongyu verkoopt voor deze banen puur calciumoxide.
Calciumoxide mengt zich met water om calciumhydroxide te maken. Calciumhydroxide is zachter en mengt beter in water. Beide zijn belangrijk voor het bouwen en helpen van het milieu.
Calciumoxide kan uw huid, ogen en longen hinderen. Mensen moeten bij gebruik handschoenen, een veiligheidsbril en maskers dragen. Changshu Hongyu gebruikt strenge veiligheidsregels om mensen veilig te houden en goede producten te maken.
De meeste fabrieken gebruiken kalksteen als hoofdmateriaal. Kalksteen bevat calciumcarbonaat. Bij het verwarmen van kalksteen ontstaan calciumoxide en kooldioxide. Dit heet calcineren.
Klanten kunnen naar de website van Changshu Hongyu gaan om calciumoxide en andere producten te kopen. Het bedrijf levert goede service en helpt kopers over de hele wereld.